د پارا مرکباتو غبرګون
فلزي پارا او د هغې مرکبات د ژوندیو موجوداتو لپاره خورا زهرجن دي. دا په ځانګړې توګه د مرکباتو لپاره ریښتیا ده چې په اوبو کې خورا محلول کیږي. د دې ځانګړي عنصر ترکیبونو سره تجربه کولو پرمهال باید خورا پاملرنه وشي (پارا یوازینی فلز دی چې د خونې په حرارت کې مایع دی). د کیمیا د بنسټیزو اصولو سره مطابقت؟ تاسو ته اجازه درکوي په خوندي ډول د پارا مرکباتو سره ډیری تجربې ترسره کړئ.
په لومړۍ تجربه کې، موږ د المونیم املګام (د دې فلز حل په مایع پارا کې) ترلاسه کوو. مرکري (II) محلول Hg نايټریټ (V) Hg (NO3)2 او د المونیم تار یوه ټوټه (عکس 1). د المونیم راډ (د زیرمو څخه په احتیاط سره پاک شوی) په ټیسټ ټیوب کې د محلول پارا مالګې محلول سره ځای په ځای شوی (عکس 2). د یو څه وخت وروسته، موږ کولی شو د تار له سطحې څخه د ګاز بلبلونو خوشې کیدو مشاهده کړو (عکس 3 او 4). د محلول څخه د راډ له لرې کولو وروسته، دا معلومه شوه چې خاوره د فلزي پوښ سره پوښل شوې، او سربیره پردې، موږ د فلزي پارا بالونه هم ګورو (عکس 5 او 6).
کیمیا - د پارا د ترکیب تجربه
د نورمال شرایطو لاندې، د المونیم سطحه د المونیم اکسایډ د کلک مناسب پرت سره پوښل کیږي.2O3فلز په مؤثره توګه د چاپیریال د تیریدونکي اغیزو څخه جلا کوي. د پارا مالګې په محلول کې د راډ پاکولو او ډوبولو وروسته، Hg آئنونه بې ځایه کیږي2+ ډیر فعال المونیم
د راډ په سطحه زیرمه شوي عطارد د المونیم سره یو املګام جوړوي، کوم چې د اکسایډ لپاره دا ستونزمن کوي چې دا یې تعقیب کړي. المونیم یو ډیر فعال فلز دی (دا د اوبو سره عکس العمل د هایدروجن خوشې کولو لپاره - د ګاز بلبلونه لیدل کیږي) او د ساختماني موادو په توګه کارول د کثافت اکسایډ پوښ له امله ممکن دي.
په دویمه تجربه کې، موږ به د امونیم NH آیون کشف کړو.4+ د نیسلر ریجنټ کارول (جرمن کیمیا پوه جولیوس نیسلر لومړی کس و چې په 1856 کې یې په تحلیل کې کارولی و).
د هپس او پارا مرکباتو عکس العمل تجربه کړئ
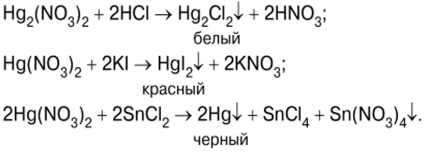
ازموینه د پارا (II) iodide HgI باران سره پیل کیږي.2د پوتاشیم آیوډیډ KI او پارا (II) نایټریټ (V) Hg (NO) د محلولونو له مخلوطولو وروسته3)2 (7 انځور):
د HgI نارنجي - سور باران2 (انځور 8) بیا د پوټاشیم آیوډیډ د اضافي محلول سره درملنه کیږي ترڅو د K فارمول محلول پیچلي مرکب ترلاسه کړي.2HgI4 ؟ د پوتاشیم تیترایوډرکوریټ (II) (عکس 9) چې د نیسلر ریجنټ دی:
د پایله شوي مرکب سره، موږ کولی شو د امونیم ایون کشف کړو. د سوډیم هایدروکسایډ NaOH او امونیم کلورایډ NH حلونه به لاهم اړین وي.4Cl (عکس 10). د نیسلر ریجنټ ته د امونیم مالګې لږ مقدار حل کولو وروسته او د قوي بیس سره مینځنۍ الکل کولو وروسته ، موږ د ټیسټ ټیوب مینځپانګې ژیړ - نارنجي رنګ رامینځته کول ګورو. اوسنی غبرګون په لاندې ډول لیکل کیدی شي:
په پایله کې د پارا مرکب یو پیچلي جوړښت لري:
د نیسلر خورا حساس ازموینه په اوبو کې د امونیم مالګې یا امونیا حتی نښو موندلو لپاره کارول کیږي (د بیلګې په توګه د نل اوبه).

